A polêmica da radioatividade: será que ela é boa ou ruim? (V.3, N.10, P.14, 2020)
Tempo estimado de leitura: 11 minute(s)
A descoberta da radioatividade, iniciada por W. Röntgen e seus estudos que desvelaram os raios x, mudou o rumo da ciência no século XX. Posteriormente, o entendimento da estrutura do átomo permitiu-se verificar que ele é composto por partículas que podem ser ejetadas de forma espontânea. A manipulação da estrutura do átomo levou, entre outras coisas, ao projeto Manhattan na cidade de Los Alamos, nos Estados Unidos (Los Alamos foi fundada por causa do projeto Manhattan) e ao uso da matéria como fonte de energia em usinas nucleares, como a usina nuclear de Angra dos Reis, no estado do Rio de Janeiro.
A radioatividade já causou algumas catástrofes como a de Chernobyl, que aconteceu em 1986 na Ucrânia; a de Fukushima, no Japão em 2011; e, para não ir tão longe, o acidente de Goiânia em 1987. Por causa desses acidentes e do seu potencial destruidor, a energia nuclear vive um momento de retrocesso, pois, após o acidente de Fukushima, uma série de programas nucleares de países que usam esta fonte de energia começou a ser cancelada, procurando migrar para energias potencialmente mais limpas. Mas não nos enganemos. O uso da radioatividade não vai desaparecer assim tão rápid, pois ele ocorrede diversas formas, seja para tratamento de doenças por meio da radioterapia e outras aplicações biomédicas, ou em equipamentos de pesquisa, em metrologia, datação etc.
O átomo é composto de nêutrons, prótons e elétrons. Os prótons têm carga positiva, e os elétrons têm carga negativa. Os nêutrons, que fazem parte do núcleo, não possuem carga elétrica, mas ficam grudados aos prótons por forças chamadas de nucleares. Os elétrons são os responsáveis pelas propriedades físicas que vemos nos materiais, ou seja, se o elemento é magnético, corrosivo, metal, isolante, gás, sólido, líquido, se derrete nas nossas mãos ou se explode ao contato com água; enquanto o núcleo é o responsável pela massa dos átomos. O que determina que o oxigênio seja oxigênio é o número de prótons que ele possui no núcleo: s 8 prótons. E, se fossem 9, não seria mais oxigênio, mas flúor, e com um próton a menos, totalizando 7, seria nitrogênio. Em um átomo estável, o número de elétrons e prótons é igual e a soma das cargas elétricas é zero, e neste caso as forças de repulsão eletrostática no núcleo (cargas iguais se repelem, cargas opostas se atraem) são compensadas pelas forças nucleares. Esta força nuclear só atua no núcleo, e além desse núcleo não existe mais essa compensação de forças. Ainda, um núcleo pode ter qualquer número de nêutrons no seu núcleo porque este não possui carga e pode ficar se agrupando com os prótons já existentes, graças às forças nucleares (as mesmas que mantém os prótons presos no núcleo). Quando temos elementos com o mesmo número de prótons mas diferente número de nêutrons, estes elementos são chamados de isótopos.
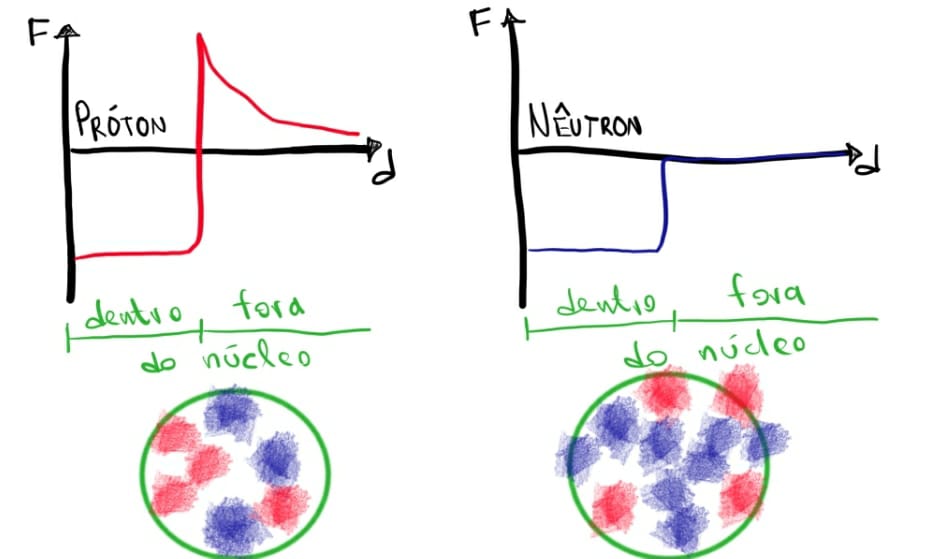
Na maioria dos casos, os isótopos têm um número de nêutrons diferente do número de prótons no núcleo. O núcleo não será tão estável se houver um desbalanço grande entre o número de prótons e nêutrons, ou se tiver muitas destas partículas no núcleo (o que acontece no caso de elementos pesados como o chumbo, o urânio e o mercúrio). Quando isto acontece, o núcleo se encontra em um estado que é frágil em termos das forças atuando nele. Dito de outra forma, todo mundo precisa caber no núcleo, e assim as forças nucleares manterão todo mundo no lugar. Se entrarem mais partículas (ou menos) do que o núcleo pode segurar, ele tentará compensar esse desbalanço de forças. Nesse processo, os núcleos se desfazem de energia, envolvendo transformações e ejeção de energia em forma de partículas.
Para saber o número de prótons e nêutrons precisamos de duas coisas: do número de prótons Z e do número de prótons e nêutrons N. Para cada isótopo, representamos estes números com a notação NXZ. Nesse caso, o isótopo de rádio (símbolo Ra) com que a Marie Curie trabalhava , por exemplo, é representado por 226Ra88, ou seja, o núcleo possui 88 prótons e 138 (226-88) nêutrons. Por simplicidade, os isótopos são representados apenas com o número N (226Ra).
O decaimento radioativo, aquele processo em que o núcleo se desfaz do que o está incomodando, é um processo aleatório, mas cada isótopo radioativo tem um tempo característico no qual a quantidade destes isótopos radioativos cai para a metade, e este tempo é chamado de tempo de meia vida. Este tempo é muito importante. Para entendermos o porquê, basta pensarmos nos cadernos e anotações do laboratório da Marie Curie. Esses objetos estão contaminados com o isótopo com o qual ela trabalhava na época, o 226Ra. A meia vida deste isótopo é de 1600 anos. Isso quer dizer que, para que a quantidade de radioatividade desse caderno seja a metade da quantidade atual demorará 1600 anos. Após esses 1600 anos o caderno ainda terá radioatividade, mas aproximadamente a metade do que tem atualmente. Por outro lado, o 131I, amplamente usado em aplicações relacionadas a tratamentos da tireoide, fígado e coração, tem uma meia vida de 8 dias, o que significa que uma pessoa fazendo tratamento com este isótopo terá a metade dos isótopos em 8 dias, e após algumas semanas a quantidade de 131I estará abaixo do detectável.
Esta radioatividade, como já comentamos, já causou bastantes estragos na história da sociedade moderna. No entanto, como muitas outras descobertas da ciência, ela pode ser usada para o nosso benefício. São algumas destas aplicações:
- Radioterapia: tratamento de tumores cancerígenos usando radiação ionizante (fontes radioativas ou aceleradores de partículas).
- Marcadores radioativos para expor o funcionamento de órgãos no corpo humano e estudar suas funções biológicas.
- Datação nuclear: estimação de tempo de objetos antigos (paleontologia) ou de estrelas através do decaimento do 14C e 87Rb, respectivamente.
- Esterilização de alimentos sem comprometer a qualidade ou a possibilidade de ingestão segura.
- Detecção de incêndios com 241Am
- Baterias nucleares com 238Pu, 60Co, 90Sr, para fornecimento de eletricidade em dispositivos como a sonda Voyager, usando dispositivos termoelétricos.
- Geração de energia elétrica em usinas nucleares.
Esses radioisótopos, ao serem instáveis, eventualmente atingem um outro estado mais estável, e para atingir este estado precisam se desfazer de energia. E, para entender como o decaimento e a emissão de partículas equivale à liberação de energia, precisamos lembrar da famosa fórmula do Einstein.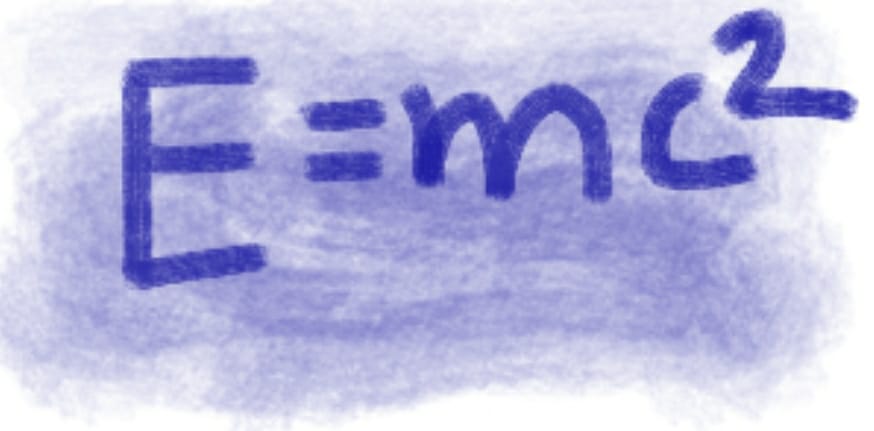 Essa fórmula estabelece uma relação entre massa e energia. Um núcleo instável, por exemplo o do 14C, emite uma partícula beta (um elétron criado no núcleo) e tem um tempo de meia vida de 5730 anos (por isto é que o teste de 14C serve para saber a idade de objetos muito antigos). Quando este núcleo, composto por 6 prótons e 8 nêutrons, decai para 12C (6 prótons e 6 nêutrons), este isótopo está se livrando da energia equivalente à massa de 2 nêutrons, só que o que realmente observamos é a emissão de uma partícula beta- (ou um elétron). Como estabelecemos a energia liberada neste decaimento? E=mc². De forma simplificada, a energia equivalente à massa desses 2 nêutrons deve ser igual à massa da partícula beta mais a energia cinética dessa partícula. Sim, a partícula beta é criada e é ejetada para fora do núcleo, e a energia cinética dessa partícula vai ser exatamente igual à energia equivalente à massa dos dois nêutrons menos a energia equivalente à massa da partícula beta. Os radioisótopos podem emitir partículas alfa (núcleos de Hélio, ou seja, núcleos com 2 prótons e 2 nêutrons), partículas beta (elétrons ou pósitrons) e partículas gamma (fótons de alta energia).
Essa fórmula estabelece uma relação entre massa e energia. Um núcleo instável, por exemplo o do 14C, emite uma partícula beta (um elétron criado no núcleo) e tem um tempo de meia vida de 5730 anos (por isto é que o teste de 14C serve para saber a idade de objetos muito antigos). Quando este núcleo, composto por 6 prótons e 8 nêutrons, decai para 12C (6 prótons e 6 nêutrons), este isótopo está se livrando da energia equivalente à massa de 2 nêutrons, só que o que realmente observamos é a emissão de uma partícula beta- (ou um elétron). Como estabelecemos a energia liberada neste decaimento? E=mc². De forma simplificada, a energia equivalente à massa desses 2 nêutrons deve ser igual à massa da partícula beta mais a energia cinética dessa partícula. Sim, a partícula beta é criada e é ejetada para fora do núcleo, e a energia cinética dessa partícula vai ser exatamente igual à energia equivalente à massa dos dois nêutrons menos a energia equivalente à massa da partícula beta. Os radioisótopos podem emitir partículas alfa (núcleos de Hélio, ou seja, núcleos com 2 prótons e 2 nêutrons), partículas beta (elétrons ou pósitrons) e partículas gamma (fótons de alta energia).
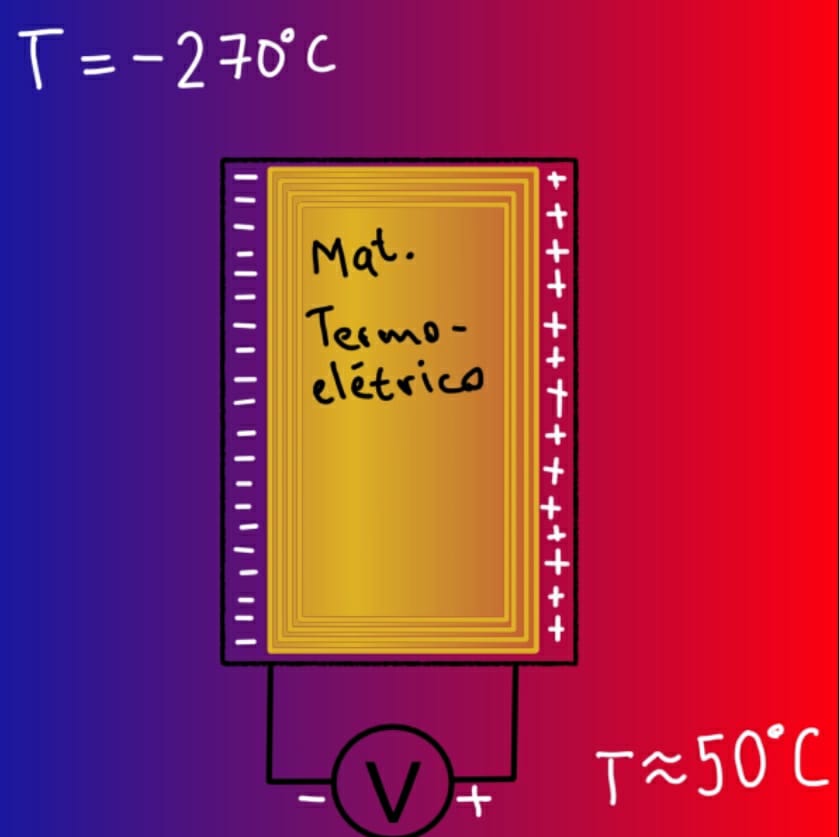
A seguinte pergunta é: o que acontece com essa partícula (alfa, beta ou gamma) após a ejeção? Bom, ela tem o universo inteiro para interagir, mas na nossa Terra, essa partícula não avança mais do que alguns centímetros ou metros sem ser espalhada por algum átomo. Quando essa partícula interage com um átomo, transfere parte da energia que carrega para ele, e esse átomo aumenta um pouco a sua energia total. Isso é muito importante para o funcionamento das baterias nucleares, já que as partículas que são produto do decaimento podem aquecer o mesmo material que o contém, como o combustível nuclear. As baterias nucleares usam radioisótopos de baixa atividade (numero menor de átomos radioativos), e os decaimentos têm o potencial de aquecer materiais próximos, devido à transferência de energia para o átomo preso numa rede cristalina, que faz com que aumente a amplitude de oscilação do átomo (o átomo chacoalhando), e portanto aumenta a temperatura do material.
Como aproveitar esse calor criado para funcionalizar o dispositivo em uma bateria? Fazendo uso de materiais termoelétricos. Os materiais termoelétricos são capazes de criar uma diferença de temperatura a partir de uma tensão elétrica, ou vice-versa: criar uma tensão elétrica a partir de uma diferença de temperatura. O efeito Seebeck é o responsável por esse fenômeno: ao existir uma diferença de temperatura em um material, os elétrons tendem a aumentar sua densidade na região que está a uma temperatura menor, criando uma diferença de carga elétrica entre a região fria e quente do material, e esta diferença de carga corresponde a uma voltagem.
 Uma das grandes dificuldades associadas à fabricação de materiais termoelétricos é a eficiência, pois geralmente é baixa. Um material termoelétrico ideal seria aquele que permitisse uma alta mobilidade dos elétrons (boa condutividade elétrica) e que não fosse eficiente na troca de calor (condutividade térmica ruim), para preservar a diferença de temperatura dentro do material. Como os elétrons geralmente estão envolvidos também na troca de calor, isto quer dizer que um material com boa condutividade elétrica também é um bom condutor térmico. Além deste inconveniente, as vibrações dos átomos que compõem o material também contribuem para conduzir calor.
Uma das grandes dificuldades associadas à fabricação de materiais termoelétricos é a eficiência, pois geralmente é baixa. Um material termoelétrico ideal seria aquele que permitisse uma alta mobilidade dos elétrons (boa condutividade elétrica) e que não fosse eficiente na troca de calor (condutividade térmica ruim), para preservar a diferença de temperatura dentro do material. Como os elétrons geralmente estão envolvidos também na troca de calor, isto quer dizer que um material com boa condutividade elétrica também é um bom condutor térmico. Além deste inconveniente, as vibrações dos átomos que compõem o material também contribuem para conduzir calor.
Existem vários materiais que mesmo com essas dificuldades são termoelétricos que permitem a criação de dispositivos para aplicações tecnológicas, como aquela de aproveitar a energia gerada por rejeitos radioativos em um dispositivo que a partir de uma diferença de temperatura possa criar uma voltagem. Esses materiais são usualmente semicondutores compostos de chumbo, bismuto, materiais com estruturas cristalinas complexas como as skuterruditas, óxidos, materiais orgânicos, e materiais baseados em silício e germânio. Esses materiais podem ter estruturas cristalinas complexas, ou serem nanoestruturas, ou materiais amorfos. Em geral, esses materiais possuem propriedades físicas bastante complexas, onde interações eletrônicas de diversas naturezas estão envolvidas e levam a comportamentos inusitados ou fortemente dependentes de outras grandezas físicas, e por isso são chamados de materiais quânticos. Este tipo de materiais é assunto de pesquisa do grupo de materiais quânticos da UFABC.


























Adorei o conteúdo dos textos. Pretendemos realizar podcast como meio para divulgação científica