Células-Tronco e a Visão do Futuro (V.7, N.11, P.01, 2024)
Tempo estimado de leitura: 9 minute(s)
A retina é um neuroepitélio complexo e de alto metabolismo, com uma variedade de células funcionando de forma integrada para receber as informações luminosas. Dada sua complexidade, também existe uma grande quantidade de retinopatias que acometem este órgão de diferentes maneiras, podendo ocasionar cegueira parcial ou total.
Dentre as afecções que acometem a retina, a retinose pigmentar (RP) é a retinopatia hereditária mais comum que induz a perda da visão, com mais de 200 genes associados ao distúrbio, afeta 1 a cada 750 a 9000 pessoas no mundo. Dentre as mutações autossômicas recessivas associadas à RP, as mais comuns são no gene da fosfodiesterase-6 (PDE6B) e no gene da RPE65. Ambas são enzimas que participam da fototransdução, processo de transformação da luz em sinais químicos que serão interpretados pelo cérebro. No geral essa doença se desenvolve ao longo de décadas, provocando alterações na retina como estresse metabólico e oxidativo, inflamação e redução da camada externa nuclear, composta pelos núcleos das células fotorreceptoras, além da retração dos segmentos dos fotorreceptores (Figura 1A, B).
Diferentemente da RP, cujo quadro de déficit visual se inicia principalmente em jovens adultos, a degeneração macular associada à idade (age related macular degeneration, AMD) é a principal causa de perda de visão irreversível em idosos. Afeta a mácula, uma região na retina responsável pela visão central, alta resolução e reconhecimento de cores. São fatores de risco, além da idade avançada, principalmente o estresse oxidativo, fatores genéticos e inflamação. É caracterizada por um acúmulo de detritos celulares, gerando um depósito de cor amarela na mácula e na retina periférica. Isso ocorre pois, com o envelhecimento, as células do epitélio pigmentar da retina (RPE) se tornam ineficientes em eliminar através da fagocitose os segmentos dos fotorreceptores, levando a um acúmulo de dejetos que pode levar à morte celular da RPE. Além disso, afeta o aporte sanguíneo, prejudicando o transporte de fluidos e levando a alterações que impactam no funcionamento das células da retina. Existem dois tipos de degeneração macular, o primeiro deles é a AMD úmida em que há a presença de fluidos ou hemorragias retinianas e apresenta uma degeneração da RPE mais rápida que a AMD seca, caracterizada por uma atrofia geográfica e alteração de pigmentação da mácula (Figura 1B).
Diferente dos distúrbios já vistos, o glaucoma afeta outro tipo de célula da retina, as células ganglionares. Trata-se de uma doença que acomete cerca de 3,5% da população de indivíduos entre 40 e 80 anos, e por se apresentar assintomática inicialmente, dificulta um diagnóstico e tratamento precoce, o que leva frequentemente a um prognóstico negativo. O glaucoma é uma doença multifatorial que envolve o aumento anormal da pressão intraocular, o que resulta na compressão das células ganglionares (Figura 1B).
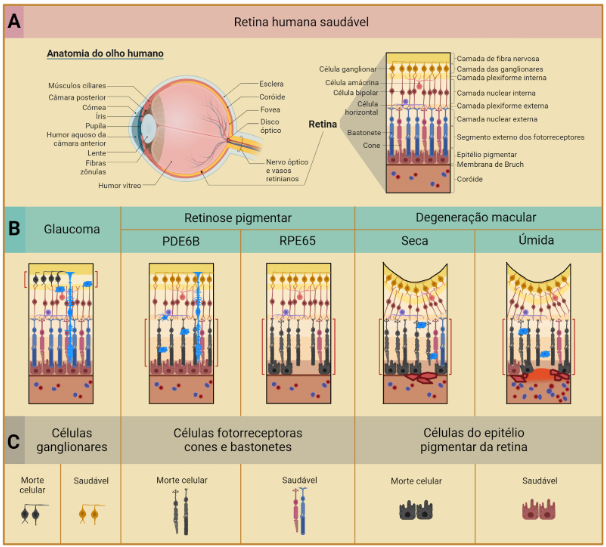
Figura 1: (A) Representação da retina humana saudável, localizada na região mais interna do globo ocular. Ao lado esquerdo, a anatomia geral do olho humano. Ao lado direito, a morfologia das células presentes na retina, separadas por camadas. (B) Morfologia característica de cada retinopatia com as células que estão em processo de morte celular em destaque cinza escuro e as camadas afetadas destacadas em vermelho. Outras células envolvidas no processo de oxidação excessiva e inflamação estão destacadas em azul claro. (C) Esquema com o principal tipo celular afetado em cada retinopatia com representação da célula no processo de morte celular vs. célula saudável. No glaucoma, as células afetadas são as ganglionares. Na retinose pigmentar, os fotorreceptores cones e bastonetes. Na degeneração macular, o epitélio pigmentar da retina.
A busca por soluções para essas doenças impulsiona a pesquisa científica em diversas frentes. Entre as áreas mais promissoras, a terapia celular surge como uma esperança de restaurar a função visual em pacientes com retinopatias de diferentes origens. Por muito tempo, a terapia com células-tronco dependia apenas das células-tronco embrionárias (embryonic stem cells, ESCs), o que levou a limitações no seu avanço devido a questões éticas e alta taxa de desenvolvimento de tumores. Contudo, com a descobertas dos fatores de Yamanaka e reprogramação celular em células pluripotentes induzidas (induced pluripotent stem cells, iPSC), foi possível progredir nos tratamentos e transplantes autólogos.
As células-tronco são células que têm a capacidade de se diferenciar em diversos tipos celulares especializados, como células do sangue, neurônios, músculos, entre outros. iPSCs são células-tronco derivadas de células adultas reprogramadas geneticamente para recuperar sua capacidade de se diferenciar em qualquer tipo de célula no corpo humano. Esta característica torna as iPSC vantajosas, pois são colhidas do próprio paciente, minimizando o risco de rejeição. No caso de degeneração retiniana, essas células podem diferenciar-se em células da retina, fotorreceptores, células bipolares, células ganglionares e células de Müller para depois serem inseridas na retina (Figura 2).
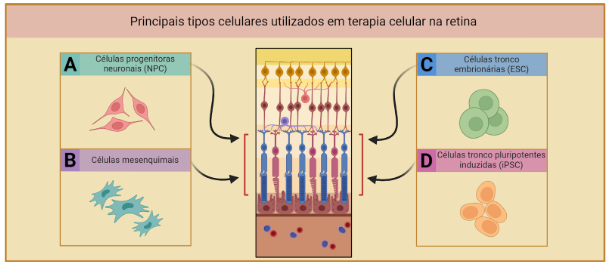
Figura 2: Principais tipos celulares utilizados em terapia celular na retina. Essas terapias são entregues na camada nuclear externa da retina (outer nuclear layer, ONL), onde estão localizados os núcleos dos fotorreceptores cones e bastonetes. Alguns tipos celulares podem ser usados em terapia conjunta. (A) Células progenitoras neuronais (neural progenitor cells, NPC). (B) Células mesenquimais. (C) Células-tronco embrionárias (embryonic stem cells, ESC). (D) Células-tronco pluripotentes induzidas (induced pluripotent stem cells, iPSC).
Em pacientes com retinopatias, a terapia celular exige métodos de entrega das células à retina, os quais podem ser realizados de duas maneiras: através da suspensão celular ou da folha celular, que consiste em uma camada contínua de células. Ambas as técnicas são aplicadas no espaço sub-retiniano, localizado abaixo da retina. A principal distinção entre elas é que a suspensão celular é administrada por meio de injeção, enquanto a folha celular é posicionada na região. É neste contexto que as terapias gênicas são implementadas em combinação a outros métodos. A entrega de células-tronco na região, por exemplo, é uma ótima estratégia a ser utilizada, porque muitas das distrofias retinianas têm origem genética e essas técnicas em conjunto incluem suplementação, modificação e/ou correção de genes.
Outra estratégia envolvendo terapia celular é a utilização de células de Müller. Essas células são abundantes na retina e desempenham diferentes funções como suporte neuronal e defesa imunológica. Em algumas espécies, elas são capazes de se diferenciar no tipo de célula que está danificada, mas em mamíferos isso não acontece. Esse mecanismo vem sendo explorado para tratar as distrofias da retina em humanos, porém há uma alta taxa de rejeição. Para diminuir essa taxa, os cientistas começaram a utilizar células de Müller advindas de organoides retinianos, estruturas tridimensionais, cultivadas em laboratório e derivadas de células-tronco, que mimetizam a organização e a função da retina humana.
Além disso, tem-se a terapia optogenética, método que insere moléculas sensíveis à luz nas células sobreviventes da retina, permitindo excitabilidade neuronal, redistribuição de proteínas e resposta à luz, sendo capaz de restaurar a visão na degeneração retiniana avançada.
A bioimpressão 3D (3DB) é outra abordagem para as retinopatias. Ela consiste na deposição de camada por camada de biomateriais com células específicas, podendo variar em diversos parâmetros como a resolução, precisão, velocidade e viabilidade celular. A 3DB já foi capaz de construir uma estrutura semelhante a da retina e, portanto, apresenta um alto potencial para ser utilizada no tratamento dessas doenças.
Vale lembrar que, mesmo alguns resultados apresentando melhora da morfologia da retina e da acuidade visual, ainda existem desafios, como a rejeição e a formação de tumores, que precisam ser considerados para garantir o sucesso clínico dessas terapias. A jornada da terapia celular para retinopatias vai além de avanços científicos. Ela representa uma batalha contra a perda da visão, um dos maiores medos da humanidade. A esperança reside na possibilidade de restaurar a capacidade de enxergar, permitindo que pessoas desfrutem das cores do mundo, reconheçam rostos queridos e vivenciem a beleza da vida com seus próprios olhos.
Referências
Bovi dos Santos, G., de Lima-Vasconcellos, T.H., Móvio, M.I. et al. New Perspectives in Stem Cell Transplantation and Associated Therapies to Treat Retinal Diseases: From Gene Editing to 3D Bioprinting. Stem Cell Rev and Rep (2024). https://doi.org/10.1007/s12015-024-10689-4