PETases – Emprego da biotecnologia na hidrólise do plástico PET (V.6. N.5. P.7, 2023)
Tempo estimado de leitura: 6 minute(s)
Os materiais plásticos derivados de petróleo vêm sendo utilizados pela humanidade há mais de um século e permeiam todos os aspectos da vida moderna, devido ao seu baixo custo de produção, alta durabilidade, resistência e impressionante versatilidade [1]. Os principais polímeros derivados de petróleo utilizados para a produção de plásticos economicamente importantes são o poliuretano (PU), o polietileno (PE), a poliamida (PA), o polietileno tereftalato (PET), o poliestireno (PS), o cloreto de polivinil (PVC) e o polipropileno (PP) [2]. O PU é encontrado em roupas e colchões, o PE é muito empregado em embalagens e revestimentos de cabos elétricos, a PA é comumente conhecida como náilon, o PET está presente em embalagens, o PS é conhecido como isopor, o PVC é utilizado na fabricação de canos e calçados e o PP encontrado em tecidos e consoles de carros. Os materiais plásticos são essenciais para as áreas da saúde e automobilística, por exemplo [2]. Na área da saúde, o uso de materiais plásticos permite o controle na transmissão de doenças, já que o mesmo é um material barato de uso individual e pode ser facilmente esterilizado e descartado. Já na área automobilística, a introdução desses tipos de materiais em veículos diminui seu custo e seu peso, o que aumenta a sua eficiência energética.
Originalmente desenvolvidos para evitar a utilização de produtos de origem animal, os plásticos se tornaram agora tão difundidos que sua liberação na biosfera e o acúmulo em aterros sanitários estão criando uma crise ambiental em escala global sem precedentes. Decerto, plásticos são encontrados amplamente em todos os oceanos da Terra, no solo e, mais recentemente, microplásticos foram observados arrastados no ar [3]. A liberação de materiais plásticos no meio ambiente em escala planetária levou à descoberta subsequente de múltiplos sistemas biológicos capazes de degradar polímeros produzidos pelo homem para uso como fonte de carbono e energia. Esses sistemas de degradação de materiais plásticos oferecem um ponto de partida para aplicações da biotecnologia rumo a uma economia circular de materiais (a economia circular associa o desenvolvimento econômico a um melhor uso dos recursos naturais).
Entre os polímeros sintéticos fabricados atualmente, o PET é o mais abundante, feito de ácido tereftálico (TPA) derivado do petróleo e etilenoglicol (EG). A durabilidade e outras propriedades físicas favoráveis tornaram o PET um dos plásticos mais amplamente utilizados na Terra. Dada à prevalência de enzimas esterases na Natureza, à biodegradação de PET tem sido muito estudada por quase duas décadas, com várias enzimas cutinases descritas com capacidade de realizar a despolimerização [4].
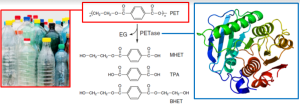
Figura: Esquerda: a garrafa PET é composta de polietileno tereftalato (PET), um polímero de alta massa molecular feito de ácido tereftálico (TPA) e etilenoglicol (EG). Direita: a bactéria I. sakaiensis revelou uma enzima PETase que ataca o polímero PET. Estrutura cristalográfica da PETase da I. sakaiensis (PDB 5XG0, https://www.rcsb.org/structure/5XG0). Centro: ao hidrolisar o PET, a enzima produz ácido mono-(2-hidroxietil) tereftálico (MHET), ácido tereftálico (TPA) e bis-2(hidroxietil) tereftalato (BHET). O produto solúvel MHET é posteriormente hidrolisado pela enzima MHETase para produzir TPA e EG. Figura adaptada da referência [4].
As grandes quantidades de PET que são liberados e se acumulam no nosso ecossistema representam sem dúvida um grande desafio ambiental. Enzimas que atuam na hidrólise de PET, ou seja, que decompõem esse plástico em seus blocos de construção podem fornecer uma solução ecológica para o acúmulo de PET no meio ambiente. A enzima PETase de I. sakaiensis exibiu excelente desempenho na hidrólise e, portanto, possui um grande potencial na decomposição do PET como também em outras aplicações biotecnológicas.